このような悩みを持っていないだろうか。
・インスリンは知っているが、それが筋肥大にどう影響するか知りたい。
・インスリンがどうやって作用を発揮するか知りたい。
この記事では以下の悩みを解決する。
この記事の内容は以下のとおりである。
1.インスリンの作用機序を解説。
2.インスリンのアナボリック作用を解説。
インスリンは筋肥大に大きな影響を及ぼすホルモンである。
この記事ではインスリンの作用機序を解説する。なぜならインスリンに限らず健康を最適化する戦略と施策はメカニズムに基づいていないと再現性が低くなるからだ。そのためにこの記事ではインスリンの作用機序を解説する。
インスリン最適化戦略と施策はこちらで解説しているので併読をすすめる。
この記事を書いている筆者は筋トレを5年間行っており、ボディビルダーを目指し研究と実践を繰り返している筋トレオタクである。またフィットネスクラブでの勤務経験があり、初心者のシェイプアップに成功した経験もある。このような筆者がインスリンの作用機序を解説しよう。
インスリンとは
インスリン
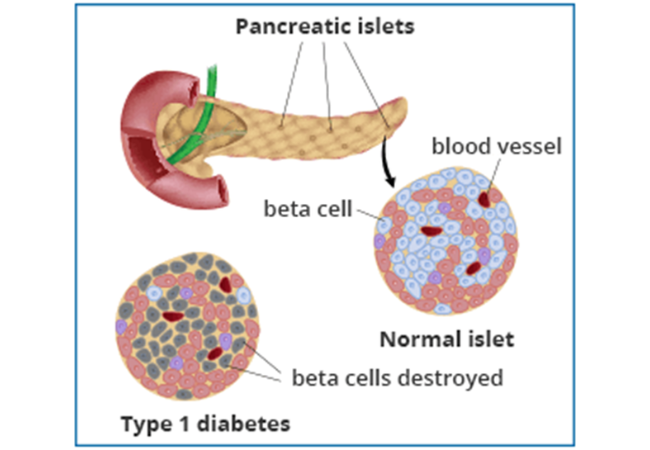
インスリンは膵臓のランゲルハンス島のβ細胞から分泌されるペプチドホルモンである。インスリンは血糖値の上昇をトリガーに分泌され、筋肉細胞、肝臓、脂肪細胞にグルコースを取り込ませることで、血糖値を低下させる作用を持つ。この過程でグルコースと共にアミノ酸も組織に取り込まれる。
インスリンは、組織内への栄養素の供給を促し、アナボリック環境整備に貢献する。この点でインスリンはアナボリックホルモンと呼ばれる。
インスリンの作用機序
1.食餌摂取
インスリンを分泌させるためには食餌を摂取する必要がある。なぜなら血糖値の上昇が分泌のトリガーだからだ。
食餌を摂取すると炭水化物が消化され、グルコースとして小腸に吸収される。こうして血中グルコース濃度が上昇し、血糖値の上昇をトリガーにランゲルハンス島β細胞が活性化し、インスリンの分泌が促進される。
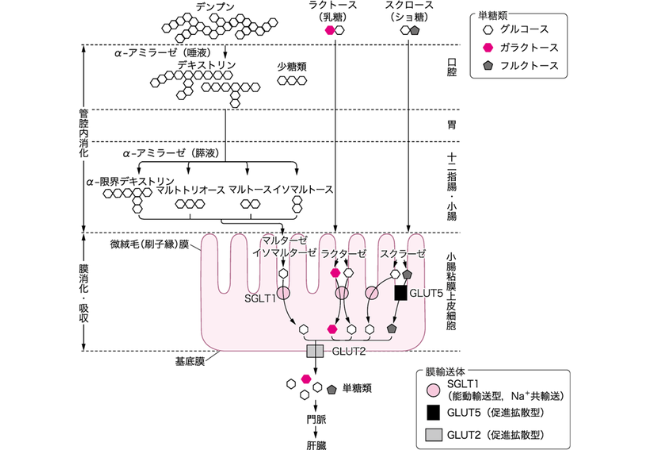
https://www.nutri.co.jp/nutrition/keywords/ch2-2/より引用。糖質の消化吸収の流れ。
インスリンは炭水化物だけでなくアミノ酸を摂取した際にも分泌される。アルギニンやチロシン、ロイシンなどはインスリン分泌作用が高いと研究で報告されている。しかしアミノ酸単体摂取では血糖値の上昇幅は小さい。なぜならアミノ酸摂取自体が血糖値を上昇させる作用を持つグルカゴン、コルチゾールなどの分泌を促進するからだ。
2.標的細胞への結合
血中に放出されたインスリンは、筋肉細胞、肝臓、脂肪細胞等の標的細胞のインスリン受容体に結合する。インスリンが受容体に結合することでシグナル伝達が開始する。
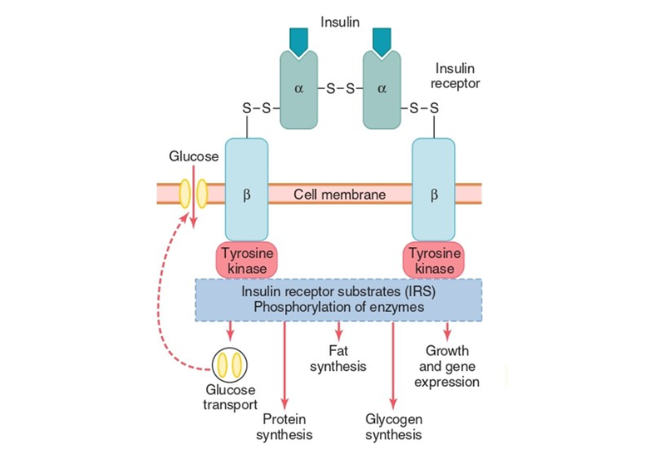
出典:Guyton and Hall Textbook of Medical Physiology 12th edition
インスリン受容体の構造。インスリン受容体は細胞膜表面でインスリンと結合するαサブユニットと、チロシンキナーゼを内在するβサブユニットから構成される。
3.グルコース取り込み
グルコースは親水性なので、通常は脂質で構成されている細胞膜に侵入することができない。しかしインスリンが受容体に結合することでグルコースが細胞内に取り込まれる。
インスリンが受容体に結合すると受容体のチロシンキナーゼが活性化する。こうしてインスリン受容体気質がリン酸化され、PI3K/Akt経路(細胞内にシグナルを伝達する経路)が活性化する。
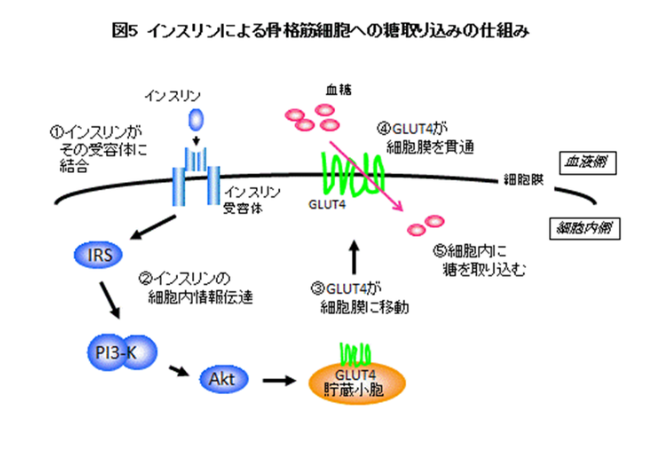
PI3K/Akt経路を通してGLUT4(グルコーストランスポーター)が細胞膜へ移動し、細胞内にグルコースが取り込まれる。GLUT4を通ってグルコースが細胞膜に取り込まれる。
https://muscle.fpark.tmu.ac.jp/Kenkyuugaiyou-detail2.htmlより引用。
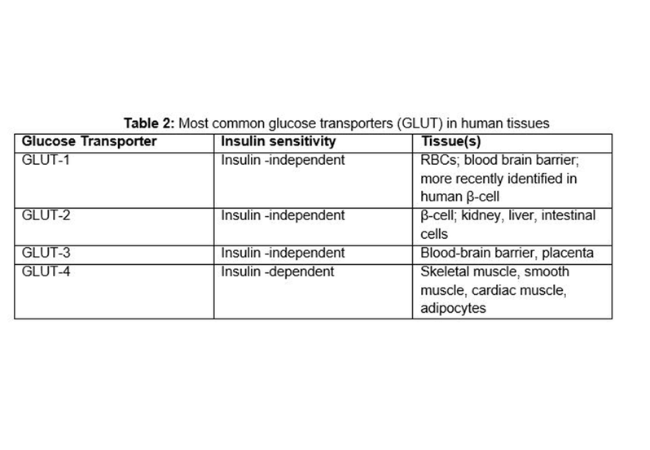
GLUTは細胞膜に存在するグルコース取り込みを司るタンパク質である。そしてインスリンが分泌されないとグルコースは筋肉細胞と脂肪細胞に運搬されない。なぜならGLUTは組織ごとに種類が存在しており、GLUT4にはインスリン依存性があるからだ。
https://pancreapedia.org/reviews/secretion-of-insulin-in-response-to-diet-and-hormonesより引用。
インスリンのアナボリック作用
筋肉細胞でのアナボリック環境整備
インスリンの作用で筋肉細胞でのタンパク質同化が促進される。なぜならインスリンによって筋肉細胞内にタンパク質同化の材料となるグルコースとアミノ酸が取り込まれるから、インスリンはPI3K/Akt/mTORシグナル伝達経路を活性化させる作用を持つからだ。
まずタンパク質合成には多くのATPが必要になる。取り込んだグルコースは解糖系によってATP生成に使用することができる。また取り込まれたアミノ酸はタンパク質同化の材料となる。
さらにインスリンはPI3K/Akt/mTORシグナル伝達経路を活性化させる。
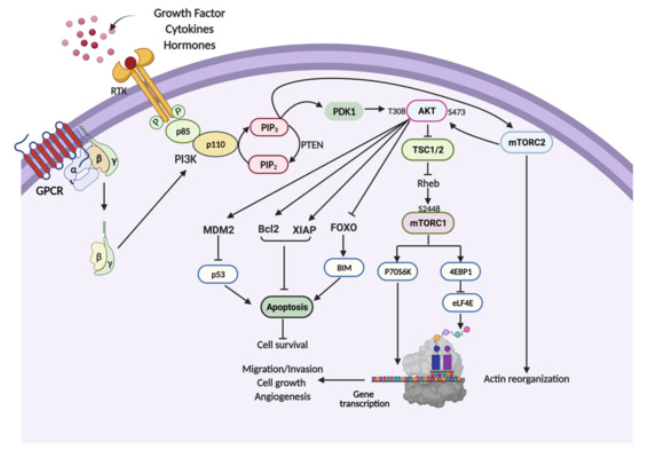
https://www.mdpi.com/1420-3049/26/13/4100より引用。PI3K/Akt/mTORシグナル伝達経路。
インスリンが受容体に結合すると自己リン酸化が起こり、IRSが活性化される。IRSはPI3K(ホスファチジルイノシトール3キナーゼ)を活性化させ、PIP2(ホスファチジルイノシトール-4,5-二リン酸)をPIP3(ホスファチジルイノシトール-3,4,5-三リン酸)に変換する。
PIP3はPDK1(3-リン酸依存プロテインキナーゼ1)をリクルートし、AKTをリン酸化して活性化させる。
TSC1/TSC2は通常、Rhebを不活性化する働きを持っているが、活性化したAKTはTSC2をリン酸化しTSC1/TSC2複合体の抑制作用を解除する。これによりRhebが活性化されmTORC1が直接活性化する。mTORC1はS6K1と4E-BP1をリン酸化し、mRNA翻訳とタンパク質合成を促進する。
AKTはmTORの活性だけでなくFOXOの抑制にも働く。AKTはFOXOをリン酸化し転写活動を抑制する。これによってFOXO由来のアポトーシスや糖新生が抑制され、細胞のカタボリックが抑制される。
以上のことから、インスリンは筋肉細胞でのタンパク質同化を促進する。
脂肪合成の促進
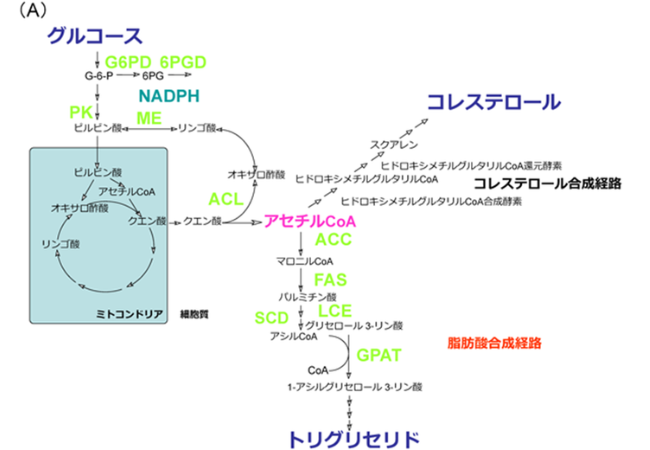
https://seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2017.890467/data/index.htmlより引用。脂肪合成のメカニズム。
脂肪細胞に取り込まれたグルコースはクエン酸回路と経てアセチルCoAに変換される。インスリンはアセチルCoAカルボキシラーゼ(ACC)を活性化させ、アセチルCoAからマロニルCoAの生成を促進する。脂肪酸合成酵素(FAS)を介して脂肪酸(パルミチン酸)が合成される。
インスリンはグリセロール-3-リン酸の供給を増加させ脂肪酸と結合し、トリグリセリドが合成される。
またインスリンはホルモン感受性リパーゼ(HSL)を抑制する作用も持ち、体脂肪の脂肪酸への分解も抑制する。
以上のことから、インスリンは脂肪合成経路を活性化させ、脂肪分解を抑制することで脂肪合成を促進させる。
最後に
この記事ではインスリンの作用と筋肥大効果を解説した。
インスリンは膵臓から分泌され、血糖値の上昇をきっかけに筋肉細胞、肝臓、脂肪細胞にグルコースを取り込ませ血糖値を下げる作用を持つ。インスリンはアナボリックホルモンとして栄養素の供給を促し、筋肉細胞でのタンパク質同化を促進する。
具体的にはPI3K/Akt/mTOR経路を活性化し、グルコースとアミノ酸が細胞内に取り込まれATPとアミノ酸がタンパク質合成に利用される。またFOXOの抑制により、アポトーシスや糖新生を抑え、細胞のカタボリックを防止する。脂肪細胞ではインスリンが脂肪合成を促進し、脂肪分解を抑制することで脂肪合成を増加させる。
次回はインスリンのメカニズムに基づいて、インスリン最適化戦略と施策を解説する。こちらを参照してほしい。











コメントを残す